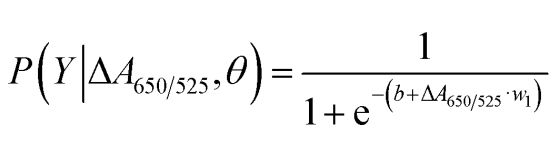液体生検に基づく癌の早期発見は、近年米国国立癌研究所によって提唱された癌の検出・診断における新たな方向性であり、早期癌や前癌病変の発見を目的としています。肺癌、消化管腫瘍、神経膠腫、婦人科腫瘍など、様々な悪性腫瘍の早期診断における新たなバイオマーカーとして広く利用されています。
メチル化ランドスケープ (Methylscape) バイオマーカーを識別するプラットフォームの出現により、がんの既存の早期スクリーニングが大幅に改善され、患者を最も早期に治療可能な段階に導く可能性があります。
最近、研究者らは、システアミン修飾金ナノ粒子(Cyst/AuNPs)とスマートフォンベースのバイオセンサーを組み合わせた、メチル化ランドスケープ検出のためのシンプルかつ直接的なセンシングプラットフォームを開発しました。このプラットフォームにより、幅広い腫瘍の迅速な早期スクリーニングが可能になります。血液サンプルからのDNA抽出後15分以内に白血病の早期スクリーニングを実施でき、その精度は90.0%です。論文タイトルは「システアミン修飾金ナノ粒子と機械学習対応スマートフォンを用いたヒト血液中の癌DNAの迅速検出」です。
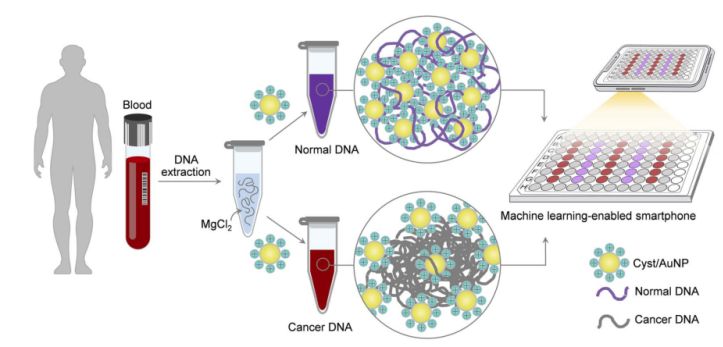
図 1. Cyst/AuNPs コンポーネントを使用した癌スクリーニング用のシンプルで高速なセンシング プラットフォームは、2 つの簡単なステップで実現できます。
これは図1に示されています。まず、水溶液を用いてDNA断片を溶解しました。次に、この混合溶液にCyst/AuNPを添加しました。正常DNAと悪性DNAはメチル化特性が異なるため、DNA断片の自己組織化パターンも異なります。正常DNAは緩く凝集し、最終的にCyst/AuNPを凝集させます。その結果、Cyst/AuNPは赤方偏移し、肉眼で赤色から紫色への色の変化が観察されます。一方、癌DNAの独特なメチル化プロファイルは、より大きなDNA断片のクラスター形成につながります。
96ウェルプレートの画像はスマートフォンのカメラで撮影されました。がんDNAは、機械学習を搭載したスマートフォンで測定され、分光法に基づく方法と比較されました。
実際の血液サンプルによるがん検査
センシングプラットフォームの有用性を高めるため、研究者らは実際の血液サンプル中の正常DNAとがん性DNAを区別することに成功したセンサーを適用した。CpG部位のメチル化パターンは、エピジェネティックに遺伝子発現を制御する。ほぼすべてのがん種において、DNAメチル化の変化、ひいては腫瘍形成を促進する遺伝子の発現の変化が交互に起こることが観察されている。
DNAメチル化に関連する他のがんのモデルとして、研究者らは白血病患者と健常対照群の血液サンプルを用いて、メチル化ランドスケープが白血病がんの鑑別診断に有効かどうかを検証しました。このメチル化ランドスケープバイオマーカーは、既存の迅速な白血病スクリーニング法よりも優れた性能を示すだけでなく、この簡便で簡便なアッセイを用いて、幅広いがんの早期発見に応用できる可能性を示唆しています。
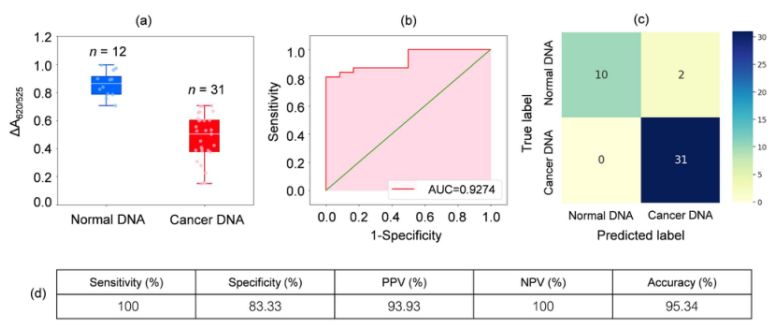
白血病患者31名と健常者12名の血液サンプルのDNAを分析しました。図2aのボックスプロットに示すように、がんサンプルの相対吸光度(ΔA650/525)は、正常サンプルのDNAよりも低くなりました。これは主に、疎水性が高まったためにがんDNAが密に凝集し、Cyst/AuNPsの凝集を妨げたためです。その結果、これらのナノ粒子はがん凝集体の外層に完全に分散し、正常DNA凝集体とがんDNA凝集体に吸着されたCyst/AuNPsの分散が異なりました。次に、閾値をΔA650/525の最小値から最大値まで変化させてROC曲線を作成しました。
図2.(a) 最適化された条件下での嚢胞/AuNPs溶液の相対吸光度値。正常DNA(青)と癌DNA(赤)の存在を示す。
(DA650/525)のボックスプロット。(b) ROC分析と診断検査の評価。(c) 正常患者と癌患者の診断のための混同行列。(d) 開発された方法の感度、特異度、陽性予測値(PPV)、陰性予測値(NPV)、および精度。
図2bに示すように、開発したセンサーで得られたROC曲線下面積(AUC = 0.9274)は、高い感度と特異性を示しました。箱ひげ図からわかるように、正常DNA群を表す最低点と癌DNA群を表す最高点の分離が不十分です。そのため、ロジスティック回帰を用いて正常群と癌群を区別しました。独立変数のセットが与えられた場合、癌や正常群などのイベントが発生する確率を推定します。従属変数の範囲は0から1です。したがって、結果は確率です。ΔA650/525に基づいて、癌同定の確率(P)を次のように決定しました。
ここで、b=5.3533、w1=-6.965です。サンプル分類では、確率が0.5未満の場合、正常サンプルであることを示し、確率が0.5以上の場合、がんサンプルであることを示します。図2cは、分類法の安定性を検証するために使用された、leave-it-aloneクロスバリデーションから生成された混同行列を示しています。図2dは、感度、特異度、陽性予測値(PPV)、陰性予測値(NPV)を含む、この方法の診断テスト評価をまとめたものです。
スマートフォンベースのバイオセンサー
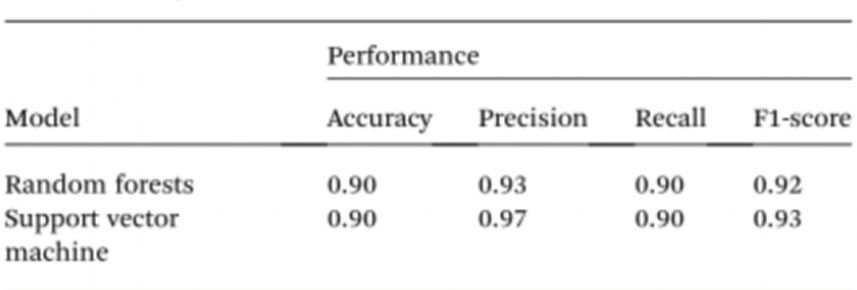
分光光度計を使わずにサンプル検査をさらに簡素化するため、研究者らは人工知能(AI)を使って溶液の色を解釈し、正常者とがん患者を区別した。これを踏まえ、携帯電話のカメラで撮影した96ウェルプレートの画像からコンピュータービジョンを使い、Cyst/AuNPs溶液の色を正常DNA(紫)またはがん性DNA(赤)に変換した。人工知能は、スマートフォンの光学ハードウェアアクセサリを使わずに、ナノ粒子溶液の色を解釈する際のコストを削減し、アクセス性を向上させることができる。最後に、ランダムフォレスト(RF)とサポートベクターマシン(SVM)の2つの機械学習モデルをトレーニングしてモデルを構築した。RFモデルとSVMモデルはどちらも、90.0%の精度でサンプルを陽性と陰性に正しく分類した。これは、携帯電話ベースのバイオセンシングにおける人工知能の使用がかなり可能であることを示唆している。
図3.(a) 画像取得ステップのためのサンプル準備中に記録された溶液のターゲットクラス。(b) 画像取得ステップ中に撮影された画像の例。(c) 画像(b)から抽出された96ウェルプレートの各ウェルの嚢子/AuNPs溶液の色強度。
研究者らは、Cyst/AuNPsを用いて、メチル化ランドスケープ検出のための簡便なセンシングプラットフォームと、白血病スクリーニングのための血液サンプルを用いた際に正常DNAと癌DNAを識別できるセンサーの開発に成功しました。開発されたセンサーは、血液サンプルから抽出したDNAを用いて、白血病患者の微量癌DNA(3nM)を15分で迅速かつ費用対効果の高い方法で検出できることを実証し、95.3%の精度を示しました。分光光度計を必要とせずサンプル検査をさらに簡素化するために、機械学習を用いて溶液の色を解釈し、携帯電話で撮影した写真から正常者と癌患者を識別し、90.0%の精度も達成しました。
参照: DOI: 10.1039/d2ra05725e
投稿日時: 2023年2月18日
 中文网站
中文网站